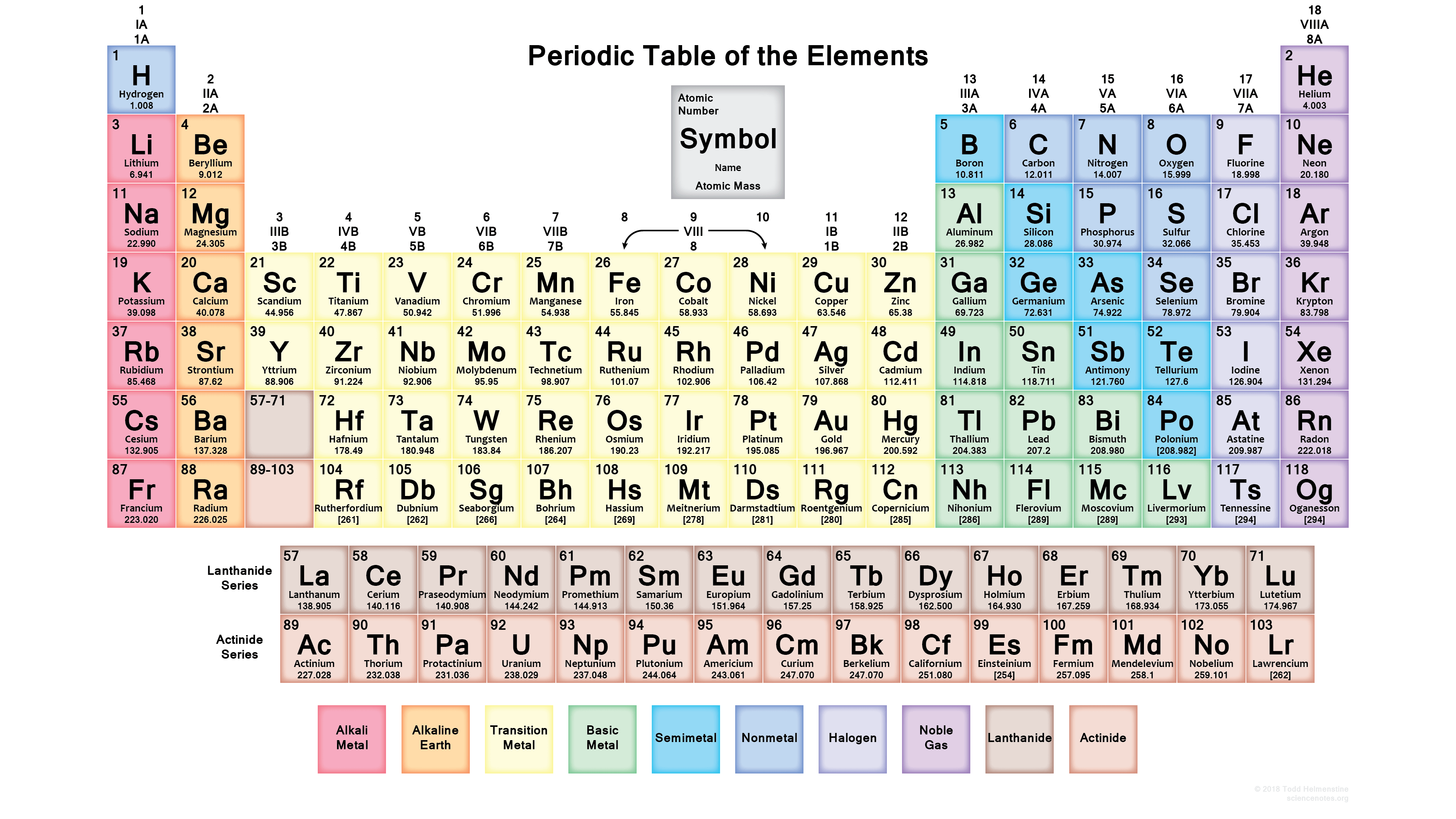
La colonna arancione è il gruppo dei metalli alcalino terrosi.
L’ultima colonna a destra è formata da gas nobili.
La penultima colonna rappresenta il gruppo degli alogeni.
Gli elementi gialli al centro della tavola si dicono metalli di transizione (vanno dal terzo al tredicesimo gruppo).
Gli elementi azzurri sono i metalloidi, o elementi di transizione, i quali hanno proprietà chimiche intermedie tra metalli e non metalli.
I metalli sono elementi con pochi elettroni di valenza, bassa energia di ionizzazione e quindi bassa affinità elettronica, quindi tendono a cedere più facilmente elettroni quando devono reagire con non metalli o metalloidi, formando cationi. Sono generalmente allo stato solido a temperatura ambiente, anche se esistono eccezioni come il Mercurio. Inoltre sono, generalmente, duttili, malleabili, lucenti conduttori elettrici, molto densi e con punti di fusione alti. Le caratteristiche dei metalli diventano meno marcate quando si procede lungo un PERIODO (riga) e sono più marcate quando si scende lungo un GRUPPO (colonna).
I non metalli sono elementi con caratteristiche opposte a quelle dei metalli, infatti hanno molti elettroni di valenza, hanno alta energia di ionizzazione ed alta affinità elettronica, quindi tendono ad acquistare più facilmente gli elettroni, formando anioni. Queste sostanze non sono duttili, malleabili,buoni conduttori o lucenti.
I semimetalli assumono il ruolo di non metallo se reagiscono con un metallo. I semimetalli assumono il ruolo di metallo se reagiscono con un non metallo.